Применение сибутрамина (Меридиа) у больных с ожирением и нарушением функции яичников.
|
Данные эпидемиологических исследований свидетельствуют о неуклонном росте частоты ожирения во всех экономически развитых странах, превышающей 10% за последнее десятилетие [24, 28]. Ожирением страдает 20-30% взрослого населения стран Европы, в связи с чем оно представляет собой серьезную медико-социаль ную проблему.
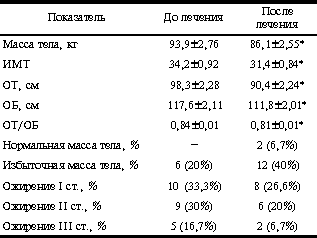
Хорошо известно, что ожирение является фактором высокого риска развития атеросклероза, ишемической болезни сердца, артериальной гипертензии, а также сахарного диабета II типа, что нередко приводит к инвалидизации и уменьшению продолжительности жизни населения [2, 10, 23]. Ожирение оказывает также неблагоприятное влияние на репродуктивное здоровье женщин. Установлена взаимосвязь ожирения с нарушениями функции яичников, проявляющимися ановуляцией, нарушением ритма менструаций, бесплодием [3, 4, 21]. Ожирение увеличивает риск развития гиперплазии и рака эндометрия [5, 7]. При абдоминальном типе отложения жировой клетчатки вероятность развития рака эндометрия может увеличиваться в 6 раз [9]. Абдоминальное ожирение рассматривается в качестве одного из основных патогенетических факторов и компонентов метаболического синдрома, патогенетическую основу которого составляет инсулинорезистентность (ИР) и гиперинсулинемия (ГИ). В научной литературе последних лет опубликовано большое число работ, посвященных взаимосвязи гиперинсулинемии с яичниковой гиперандрогенией [8, 11, 26]. Большинством исследователей признается, что ИР и ГИ способствуют формированию синдрома поликистозных яичников (СПКЯ) [17, 18, 21, 25].У пациенток с абдоминальным ожирением частота ГИ на фоне СПКЯ в два раза превышает таковую у женщин с нормальной массой тела и достигает 70-75% [15]. В связи с этим лечение ожирения несомненно является важным звеном в комплексе лечебных мероприятий, проводимых больным с нарушением функции яичников. Наряду с немедикаментозными методами воздействия важная роль в лечении больных с ожирением отводится фармакотерапии. Одним из препаратов нового поколения является сибутрамин - селективный ингибитор обратного захвата нейромедиаторов - серотонина и норадреналина в синапсах центральной нервной системы. Препарат обладает двойным механизмом действия, приводя к снижению потребности в приеме пищи и повышению термогенеза [1, 29]. Целью исследования явилась оценка эффективности терапии сибутрамином у женщин репродуктивного возраста с ожирением и нарушением функции яичников. Материал и методы В исследование было включено 30 женщин в возрасте от 21 года до 43 лет (средний возраст 31,3±1,13 года), имеющих ожирение (ИМТ > 27) и различные нарушения функции яичников. Степень выраженности ожирения определяли по величине ИМТ. Так, у 6 (20%) больных была диагностирована избыточная масса тела (ИМТ < 30), у 10 (33%) - ожирение I степени (ИМТ 30-35), у 9 (30%) - ожирение II степени (ИМТ 35-40) и у 5 (16,7%) - ожирение III степени (морбидное, ИМТ > 40). Подавляющее большинство больных - 24 (80%) - имело абдоминальный тип ожирения, при этом величина индекса, отражающего отношение окружности талии к окружности бедер (ОТ/ОБ) превышала 0,8, средний показатель ОТ/ОБ составил 0,84±0,01. Длительность ожирения в среднем составила 11,5±1,19 лет. У всех больных были выявлены различные нарушения функции яичников. У 25 (83,3%) больных отмечалась олигоменорея в виде задержек менструаций различной степени длительности: у 8 - задержки менструаций не превышали 1 мес, у 11 колебались от 1 до 3 мес и у 6 - от 3 до 6 мес. У 5 (16,7%) больных менструальный цикл был регулярным, при этом у одной имела место недостаточность лютеиновой фазы цикла (НЛФ) и у 4 - ановуляция. Средняя длительность нарушений менструального цикла составила 10,6±1,87 лет. У подавляющего большинства больных - у 25 (83,3%) - отмечалось первичное или вторичное бесплодие. Клинические признаки андрогенизации имелись у 22 (73,3%) больных, среднее значение гирсутного числа по шкале Ферримана - Голлвея было равно 15,8±1,31. У 23 больных при УЗИ было выявлено увеличение размеров яичников и эхографические признаки СПКЯ. На яичниковую гиперандрогению указывало повышение уровня тестостерона, выявленное у этих больных. У больных, включенных в исследование, не был диагностирован сахарный диабет и гипертоническая болезнь, у 7 (23,3%) отмечалась ВСД по гипертоническому типу. С целью снижения массы тела всем пациенткам проводилась терапия сибутрамином (меридиа, «Knoll AG», Германия). Начальная суточная доза для всех больных составляла 10 мг. В тех случаях, когда после 1-го месяца лечения потеря массы тела была менее 2 кг, дозу препарата увеличивали до 15 мг/сут. Общая продолжительность лечения составила 12 нед. На фоне проводимой терапии больным была рекомендована негормональная контрацепция. Ежемесячно проводилась оценка антропометрических параметров: массы тела, ИМТ, объема талии и бедер и их соотношения, а также характера менструального цикла. Функция яичников оценивалась по тестам функциональной диагностики и уровню прогестерона в сыворотке крови. Исходно и после проведенного курса лечения радиоиммунными методами с использованием тест-систем Immunotech (Чехия) или ИБОХ (Беларусь), согласно приложенным к ним инструкциям, проводилось исследование содержания в сыворотке крови больных ЛГ, ФСГ, СТГ и тестостерона (Т). Результаты исследования На фоне 12-недельного курса терапии сибутрамином у всех пациенток отмечалось снижение массы тела. Потеря массы тела после 3 мес лечения колебалась в широких пределах - от 2 до 21 кг и составила в среднем 7,8±0,72 кг, т.е. 8,2% от исходных значений. Снижение массы тела более чем на 5% было достигнуто у 25 (83,3%) больных, при этом у 8 (26,7%) из них потеря веса превысила 10%. Лишь у 5 (16,7%) больных снижение массы тела было незначительным ( < 5%). За 1-й месяц лечения потеря массы тела колебалась от 1 до 13 кг, составляя в среднем 3,3±0,48 кг (3,5%). Восемь больных (26,7%) снизили свой вес менее чем на 2 кг, в связи с этим на последующие 2 мес доза препарата им была увеличена до 15 мг/сут, что привело к более значительному снижению массы тела в последующие 2 мес терапии. Потеря массы тела за 2-й месяц лечения достоверно не отличалась от таковой в 1-й месяц (р < 0,05) и составила в среднем 2,5±0,24 кг (2,6% от исходных значений). В течение 3-го месяца терапии потеря массы тела была менее значительной - 1,97±0,22 кг (2,1%) по сравнению с предыдущими месяцами (р > 0,05). Снижение массы тела проявлялось закономерным уменьшением степени выраженности ожирения, о чем свидетельствуют данные, приведенные в табл. 1. Так, после 3-месячного курса терапии сибутрамином у двух больных масса тела уже не превышала нормативных значений, в 2 раза увеличилось число больных с избыточной массой тела, наряду с этим в 1,5-2 раза уменьшилась частота ожирения II и III степени. Снижение массы тела сопровождалось уменьшением окружности талии и бедер. Однако, если окружность талии уменьшилась в среднем на 7,2±0,55 см, то окружность бедер лишь на 5,6±0,38 см (р < 0,05). Изменение этих показателей сказалось на величине индекса ОТ/ОБ, который также достоверно снизился после 3 мес терапии (табл. 1). Таблица 1. Антропометрические показатели и степень выраженности ожирения у больных, включенных в исследование, до и после терапии сибутрамином, М±m
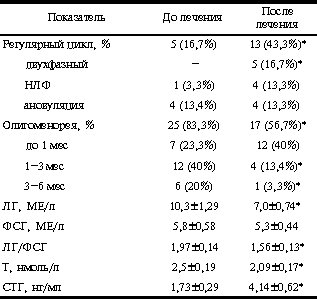
Примечание. * - достоверные различия с группой больных до лечения (р < 0,05). Наряду с улучшением антропометрических показателей положительные изменения отмечались и в характере менструального цикла. Так, если исходно регулярный цикл был лишь у 5 больных, то после лечения регуляция цикла отмечена еще у 8 (26,7%). У 18 (56,7%) пациенток сохранялась олигоменорея, однако длительность задержек менструаций значительно сократилась. Данные, представленные в табл. 2, свидетельствуют о том, что после лечения в 2 раза чаще у больных наблюдались небольшие задержки менструаций до 1 мес; наряду с этим значительно уменьшилась частота длительных задержек менструаций. Так, если до лечения задержки длительностью от 1 до 3 мес были у 40% больных, то после лечения лишь у 13,4%. Отсутствие менструаций более 3 мес, несмотря на проводимую терапию, было отмечено только у одной больной. Трехмесячный курс терапии сибутрамином оказывал существенное влияние на гормональные параметры. Как видно из данных, представленных в табл. 2, это проявлялось уменьшением среднего уровня ЛГ при неизменных показателях ФСГ, что сказалось на снижении индекса ЛГ/ФСГ. Наиболее выраженные изменения касались содержания СТГ в сыворотке крови больных с ожирением. Средний уровень данного показателя к концу курса терапии увеличился почти в 2,5 раза и составил соответственно 1,73±0,29 и 4,14±0,62 нг/мл. Так, если исходно низкие значения СТГ (1,0 нг/мл и менее) были выявлены у 14 (46,7%) больных, включенных в исследование, то послелечения ни в одном случае не было отмечено столь низких значений этого показателя. Терапия сибутрамином приводила к достоверному снижению содержания тестостерона в сыворотке крови пролеченных больных. Исходно повышенные уровни гормона были выявлены у 13 (43,3%) больных, после лечения лишь у 1 (3,33%). Учитывая различную реакцию на проводимую терапию, представилось интересным проанализировать характер менструального цикла и гормональные параметры больных в зависимости от величины потери массы тела. Как видно из данных табл. 3, снижение массы тела более 10% от исходного уровня приводило к регуляции менструального цикла у подавляющего большинства больных. Так, если до лечения у 7 из 8 больных была олигоменорея в виде задержек менструаций различной степени длительности, то после снижения массы тела нарушения цикла в виде незначительных задержек менструаций отмечались лишь у 2 больных. У 5 из пролеченных отмечался двухфазный менструальный цикл. При снижении массы тела более 10% отмечалась выраженная положительная динамика гормональных показателей. Это проявлялось достоверным снижением уровня Т и повышением концентрации СТГ в сыворотке крови пролеченных больных. При снижении массы тела на 5-10% регулярный ритм менструаций восстановился лишь у 2 из 14 больных, исходно имеющих олигоменорею. Хотя отмечалась тенденция к уменьшению длительности задержек менструаций, о чем свидетельствует увеличение числа больных с олигоменореей до 1 мес. При снижении массы тела менее 5% существенных изменений в характере менструального цикла и гормональных параметров не выявлено (табл. 3). На фоне терапии сибутрамином побочные эффекты в виде сухости во рту наблюдались у 3 (10%) больных в первые недели лечения, однако это не потребовало отмены лечения. Значимых подъемов систолического и диастолического артериального давления отмечено не было, в связи с чем не было показаний к назначению гипотензивной терапии. Обсуждение Ожирение оказывает неблагоприятное влияние на репродуктивную систему женщин, приводя к различным нарушениям функции яичников. Подтверждением этому являются данные о высокой частоте хронической ановуляции и олигоменореи у обследованных больных, имеющих различную степень ожирения. Таблица 2. Частота нарушений менструального цикла и некоторые гормональные параметры больных до и после терапии сибутрамином, М±m
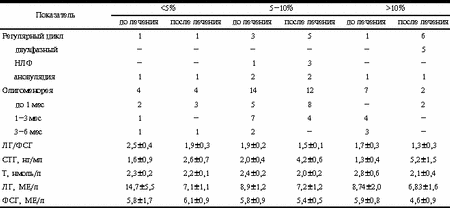
Примечание. * - достоверные различия с группой больных до лечения (р < 0,05). Таблица 3. Характер нарушений менструального цикла и некоторые гормональные параметры пролеченных больных с различной потерей массы тела, М±m
Подавляющее большинство из них имели СПКЯ, диагностированный на основании наличия клинических признаков андрогенизации, характерной эхографической картины и увеличения уровня тестостерона. Особенности гормонального фона больных, включенных в исследование, заключались также в снижении уровней СТГ. Низкие значения этого показателя характерны как для больных с ожирением, так и с СПКЯ, что может быть следствием гиперинсулинемии и повышенных концентраций ИФР-1, часто выявляемых при этих состояниях, а также результатом избыточного уровня свободных жирных кислот, оказывающих тормозящее влияние на продукцию СТГ [16, 22].Роль ожирения как патологического состояния, способствующего возникновению хронической ановуляции и нарушений ритма менструаций, можно рассматривать в нескольких аспектах. Известно, что жировая ткань является местом периферического синтеза андрогенов [4]. При ожирении увеличивается не только количество жировой ткани, но и активность ферментных систем, участвующих в биосинтезе половых стероидов, что может приводить к повышенному синтезу андрогенов [19, 21]. Абдоминальное ожирение часто сочетается с инсулинорезистентностью и гиперинсулинемией [2, 21]. Высокое содержание инсулина способствует увеличению синтеза яичниковых андрогенов, избыточное количество которых может вызывать атрезию антральных фолликулов, ановуляцию и нарушения ритма менструаций, которые были характерны для женщин с ожирением, включенных нами в исследование. В связи с этим логично предположить, что лечение ожирения может привести к снижению избыточной массы тела и оказать положительный эффект на характер менструального цикла. С этой целью был использован препарат нового поколения сибутрамин (меридиа). Результаты проведенного исследования показали, что 12-недельный курс терапии сибутрамином у 83,3% больных приводил к снижению массы тела более чем на 5%. Причем у каждой 4-й пациентки потеря массы тела превышала 10%. Снижение массы тела на 5-10% можно считать весьма успешным результатом лечения, поскольку имеются данные о том, что этого уже достаточно для уменьшения частоты развития сердечно-сосудистых заболеваний, сахарного диабета и преждевременной смертности [1]. Средняя потеря массы тела за 12-недельный период составила 7,8±0,72 кг, что существенно не отличается от данных других исследователей, использовавших сибутрамин для лечения больных с ожирением и сахарным диабетом [1, 13]. Хотя в работе Wadden приводятся цифры, свидетельствующие о более значительной потере массы тела (16,5±8,0%). Это можно объяснить как более длительным приемом препарата, так и сочетанием его с низкокалорийной диетой. Снижение массы тела сопровождалось закономерным уменьшением степени выраженности ожирения. Так, если до лечения ожирение различной степени выраженности (ИМТ і30) было диагностировано у 80% больных (20% имели предожирение или избыточный вес), то после проведенного курса терапии ожирение сохранялось лишь у 53,3% больных, у 40% больных отмечался избыточный вес, у 6,7% - масса тела не превышала нормативных показателей. Важно отметить значительное (в 2,5 раза) уменьшение частоты морбидного ожирения (ИМТ-40), которое влечет за собой развитие целого ряда соматических заболеваний и нередко является показанием для применения хирургических методов лечения. У 80% больных, включенных в исследование, был диагностирован абдоминальный тип ожирения, который является одной из основных составляющих метаболического синдрома [14]. Следует отметить, что применение сибутрамина приводило к более выраженному уменьшению объема талии по сравнению с объемом бедер, результатом этого явилось достоверное снижение коэффициента ОТ/ОБ (0,84±0,01 и 0,81±0,01) и соответственно уменьшение частоты абдоминального ожирения. Лечение сибутрамином способствовало не только снижению массы тела, но и регуляции ритма менструаций. Так, если до лечения регулярный менструальный цикл (НЛФ или ановуляцию) имели 16,7% больных, то после лечения - 40%. При этом более чем у половины из них циклы были овуляторными. У части больных, несмотря на отсутствие нормализации ритма менструаций, положительный эффект снижения массы тела выражался в уменьшении длительности задержек менструаций. Исходно задержки менструаций от 1 до 6 мес отмечались у 60% больных, в то время как после лечения лишь у 16,7%, у большинства больных длительность задержек не превышала 1 мес. В ходе исследования выявлена взаимосвязь между степенью снижения массы тела и восстановлением нарушений менструального цикла. Так, при потере массы тела на 5-10% от исходной отмечалась лишь тенденция к укорочению задержек менструаций, лишь у двух больных восстановился нормальный ритм менструаций. Наиболее существенные положительные изменения в виде восстановления регулярного цикла отмечались при снижении веса более 10% от исходных значений. Схожие данные о влиянии похудания на характер менструального цикла у женщин с ожирением были отмечены Вейнберг (1998). Хотя с ее точки зрения выраженное улучшение состояния репродуктивной системы следует ожидать при снижении веса более чем на 15%. Положительный эффект снижения массы тела на характер менструального цикла в значительной степени связан со снижением уровня яичниковых андрогенов и уменьшением блокирующего влияния их на яичник. Это подтверждают полученные нами данные о достоверном снижении содержания тестостерона в сыворотке крови на фоне терапии сибутрамином. Следует отметить, что наибольшее падение уровня тестостерона было выявлено у больных, снизивших свой вес более чем на 10%. Можно полагать, что эти эффекты препарата являются как результатом уменьшения синтеза андрогенов в жировой ткани, так и уменьшения степени выраженности гиперинсулинемии и активности ключевого фермента биосинтеза яичниковых андрогенов - цитохрома P450c17a [19]. Снижение массы тела на фоне лечения сибутрамином сопровождалось выраженным повышением (в 2,5 раза) исходно низких значений уровня СТГ, что согласуется с данными других исследователей [22]. Восстановление нормальных концентраций СТГ в плазме крови является важным этапом терапии, учитывая выраженный липолитический эффект этого гормона [12, 20]. Обобщая результаты проведенного лечения, можно заключить, что терапия сибутрамином способствует эффективному снижению массы тела, нормализации гормональных параметров и регуляции менструального цикла. Следовательно, назначение сибутрамина может рассматриваться в качестве начального этапа терапии больных с ожирением и нарушением функции яичников. Это будет оказывать корригирующее влияние как на избыточную массу тела, так и на состояние репродуктивной системы, что позволит в ряде случаев избежать гормонотерапии или отсрочить ее назначение. В.П. Сметник, Г.Е. Чернуха, Л.Г. Валуева Научный центр акушерства, гинекологии и перинатологии РАМН, Москва Литература 1. Бутрова С.А. Сибутрамин (Меридиа) в лечении ожирения: опыт применения в России. Клин фарм и тер 2001; 10: 2: 71-74. 2. Бутрова С.А. Синдром инсулинорезистентности при абдоминальном ожирении. Лечащий врач 1999; 7: 32-36. 3. Вейнберг М.Э. Некоторые показатели функционального состояния репродуктивной системы: Автореф. дис. ... … канд. мед. наук. Тбилиси 1998. 4. Стекольщикова О.Д. О нарушении периферического метаболизма половых стероидов при ожирении. Акуш и гин 1983; 9: 15-17. 5. Austin H., Austin J.M., Partridge E.E. et al. Cancer Res 1991; 51: 568. 6. Аzzis R. Fertil Steril 1989; 52: 703-725. 7. Bacer T.R. In: Handbook of Gynecologic Oncology. Еd. by M.S. Piver. 1995; 133-140. 8. Dunaif A., Givens J.R., Haseltine F., Merriam G.R. The Polycystic ovary syndrome. Blackwell Scientific. Cambridge 1992. 9. Eliott E.A., Matanoski G.M., Roseushein N.B. Oncology 1990; 32: 253. 10. Ferranini E., Haffner S.M., Mitchell B.D., Stern M.P. Diabetologia 1991; 34: 416-422. 11. Franks S. N Engl J Med 1995; 333: 853-861. 12. Gertner А. Horm Res 1993; 40: 1: 10-15. 13. James W., Astrup A., Finer N. et al. Lancet 2000; 356 (9248): 2119-2125. 14. Kaplan N.M. Arch Int Med 1989; 149: 1514-1520. 15. Mancuso S., Lanzone A., Fulgbesu A.M. et al. In Hormones in Gynecological Endocrinology. Еd. by A.R. Genazzari, I. Petraglia. Parthenon Publishing Group 1992; 439-447. 16. Matsuzawa Y., Nakamura T., Shimomura I. et al. Obes Res 1995; 3: 5: 645-647. 17. Nestler J.E. Int J Obes Relat Metab Dis 2000; 24: 71-73. 18. Nestler J.E. Semin Reprod Endocrinol 1997; 15: 2: 111-122. 19. Nestler J.E., Jakubowicz D.J. N Engl J Med 1996; 335: 9: 617-23. 20. Ortlepp J.R., Kluge R., Giesen K. et al. Eur J Clin Invest 2000; 30: 3: 195-202. 21. Pasqualy R., Gambineri A., Bisscoti D. et al. J Clin Endocrinol Metab 2000; 85: 8: 2767-2774. 22. Rosmond R., Bjorntorp P. Int J Obesity 1998; 22: 12: 1184-1196. 23. Saleh J., Sniderman A.D., Cianflone K. Clin Chim Acta 1999; 281: 1/2: 163-180. 24. Seidell J.C. The wordwide epidemic of obesity. 8th international congress on obesity. In: Guy-Grand Ailhaud G., еds. Progress in obesity research, 8th edn. London: John Libbey 1999; 661-668. 25. Taylor A.E. Am J Obstet Gynecol 1998; 179: 6: 94-100. 26. Toscano V., Bianchi P., Balducci R. et al. J Clin Endocrinol 1992; 36: 197-202. 27. Wadden T.A., Berkowitz R.I., Sawer D.B. et al. Arch Int Med 2001; 22: 161(2): 218-227. 28. WHO. Obesity: preventing and managing the global epidemic. Report of a WHO consultation on obesity. Geneva, June 3-5, 1997. Geneva 1998. 29. Wаlsh K.M., Leen E., Lean M.E. Int J Obes Relat Metab Dis 1999; 23: 10: 1009-1015. |